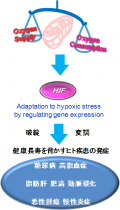
肝内代謝制御機構とその破綻による疾患発症メカニズムの解明

背景
肝臓は生体内の代謝の中心臓器であり、その機能低下は生命を脅かす。肝臓の代謝機能はホルモンなどの液性因子により制御される一方、近年自律的な制御機構も重要視されている。低酸素環境が、脂肪肝、肝炎や肝線維症などのさまざまな肝疾患において共通の基礎病態として認められ、低酸素環境への適応不全が肝代謝制御の破綻と密接に係わっていることが次第に明らかになってきている。
シーズ概要
細胞内低酸素応答機構の中心分子である転写制御遺伝子Hypoxia inducible factor (HIF)-1についての知見を有する。肝実質細胞における低酸素応答の破綻がアルコール性および非アルコール性脂肪肝の発症や進展に係わっていることを見出した。特に、アルコール性脂肪肝発症メカニズムにHIF-1による脂肪酸代謝制御の破綻が係わっていることを明らかにしている。また、HIFアイソフォームのHIF-2の関与についても研究を展開している。
応用・展開
HIFを標的とした低分子化合物を開発し、肝臓特異的にデリバリーすることで、肝疾患の発症や進展を制御できると考えられる。
優位性
ヒト疾患モデルを個体レベルで再現し、HIFによる代謝制御を介した病態発症・進展機構の解明に取り組んでいる。また、生体顕微鏡システムを用いたin vivoイメージング技術を用いて、癌細胞と宿主側の間質細胞や免疫担当細胞との相互作用の解析を行い、この相互作用における低酸素環境の病態生物学的意義についての解明にも取り組んでいる。
提供目的
受託研究、共同研究、技術相談
掲載日:
2011/10/28